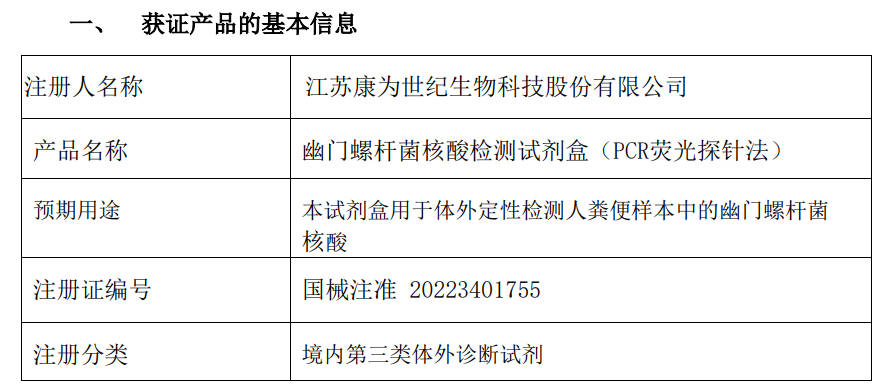
康为世纪公告,幽门螺杆菌核酸检测试剂盒(PCR荧光探针法)取得医疗器械注册证。
公司上述幽门螺杆菌核酸检测试剂盒(PCR 荧光探针法)用于体外定性检测
人粪便样本中的幽门螺杆菌核酸,用于幽门螺杆菌感染的辅助诊断。
早在 1994 年,WHO 下属的国家癌症研究机构就将幽门螺杆菌定义为 I 类致
癌原。2021 年,美国卫生及公共服务部公布的第 15 版致癌物报告中,将幽门螺
杆菌新增为明确致癌物。现已明确幽门螺杆菌的感染可导致胃炎、消化性溃疡、
消化不良乃至胃癌的发生。目前临床上主要采用 C13/C14 呼气试验、快速尿素酶
试验及粪便抗原试验等方法检测幽门螺杆菌,最新的研究显示,利用分子生物学
方法检测幽门螺杆菌具有明显的优势,不仅能检测有无幽门螺杆菌的感染,提取
出来的核酸还可用于相应的毒力因子基因及多种抗生素耐药基因的检测,可为幽
门螺杆菌的根除提供更为精准的治疗方案,提高幽门螺杆菌治疗的根除率,降低
胃癌的发生。采用粪便样本还具有无创且可居家采样的优势,消费者使用简便,
测试前无需服药或空腹,为幽门螺杆菌的大规模的筛查及后续治疗提供了更为便
捷的检测手段。
二、对公司的影响及风险提示
此次幽门螺杆菌核酸检测试剂盒是国家药监局颁发的基于粪便样本对幽门
螺杆菌的核酸检测的第 1 张 III 类证,有助于提升公司在胃癌早筛相关领域的竞
争力,不仅对公司销售及业务拓展具有积极的作用,还对我国胃癌早筛、早诊早
治具有积极的临床价值和社会意义。上述产品的实际销售情况取决于未来市场的
推广力度等多因素影响,公司尚无法预测该产品的获批对未来业绩的具体影响,
敬请广大投资者注意投资风险。