健民集团公告,通降颗粒获得《药物临床试验批准通知书》。
二、药品研发及相关情况
通降颗粒处方源于医疗机构院内制剂,功能主治为疏肝清热,和胃降逆。用于
肝胃郁热证。症见烧心,反酸,嘈杂、胸骨后疼痛,嗳气、咽部异物感、胸胁胀满
或胀痛,舌质红或略红,苔白或略黄,脉弦。适用于胃食管反流病见上述证候者。
目前通降颗粒已完成制备工艺、质量标准、稳定性及药理毒理等临床前研究。
本品处方前期作为院内制剂在临床上取得了良好疗效,尤其是在治疗胃食管反流病
肝胃郁热证方面,显示出较好的临床疗效,且未见明显不良反应,毒理试验结果也
显示,本品安全性好,安全剂量范围较宽。
公司拥有通降颗粒独立完整自主的知识产权。截至目前,公司累计研发投入
608.10万元。
三、同类药品及市场情况
中华医学会消化病学分会制订的《2020年中国胃食管反流病专家共识》指出,
胃食管反流病属消化系统常见病与多发病,是胃内容物反流入食管或者以上部位,
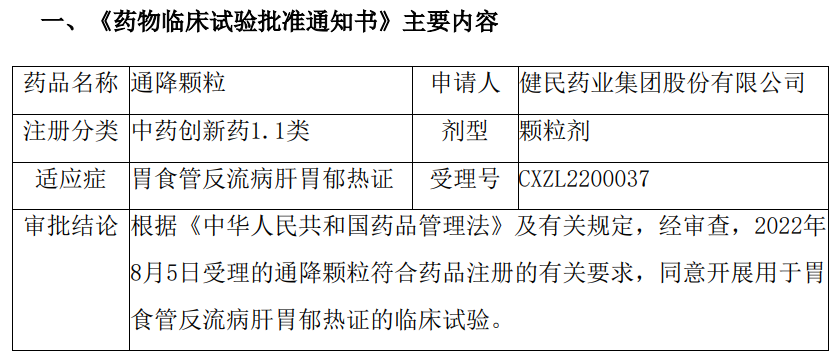
药品名称 通降颗粒 申请人 健民药业集团股份有限公司
注册分类 中药创新药1.1类 剂型 颗粒剂
适应症 胃食管反流病肝胃郁热证 受理号 CXZL2200037
审批结论 根据《中华人民共和国药品管理法》及有关规定,经审查,2022年
8月5日受理的通降颗粒符合药品注册的有关要求,同意开展用于胃
食管反流病肝胃郁热证的临床试验。
进入咽部、口腔或肺引起的不适症状和(或)并发症。流行病学资料显示,胃食管
反流病患病率在全球范围内呈上升趋势,我国胃食管反流病患病率高达1.9%~7.0%,
属于胃肠动力障碍性疾病,症状多而复杂,常重叠功能性胃肠病症状,伴焦虑、抑
郁状态,且容易反复发作,需维持用药。严重影响患者的生活质量,给患者带来重
大的经济负担。中华中医药学会脾胃病分会2017年发布的《胃食管反流病中医诊疗
专家共识意见》指出,胃失和降,胃气上逆为胃食管反流病基本病机,肝胆失于疏
泄、脾失健运、胃失和降、肺失宣肃、胃气上逆,上犯食管,形成本病的一系列临
床症状。药物治疗以中和胃酸、抑制反流为主,临床上主要以抑酸、促胃动力和胃
黏膜保护剂等药物治疗,多为化学药品,药品的品种较多。长期抑酸治疗可能导致
不良反应,症状重叠时无明确的综合治疗手段,抑酸停药后导致病情反复。通降颗
粒未来若经研发、审批并成功上市,可为胃食管反流病患者提供新的治疗选择。
四、产品上市尚需履行的审批程序
根据我国药品注册相关的法律法规要求,公司在收到《临床试验批准通知书》
后,需根据批件要求开展并完成临床试验后,整合申报资料申报生产,并经国家药
监局审评、审批通过后方可上市生产。
五、风险提示
本次通降颗粒获得药物临床试验批准,将进一步丰富公司在临床研发阶段的产
品管线;通降颗粒后续的临床试验、审评和审批的结果及时间都存在诸多不确定性,
对公司近期业绩不会产生影响;新药研发过程中产品从研制、临床试验、上市审批
到上市生产和商业化的周期长、环节多,容易受到不确定因素影响,未来产品市场
竞争形势也将发生变化;公司将按国家有关规定积极推进上述研发项目,并及时对
项目后续进展情况履行信息披露义务。敬请广大投资者谨慎决策,注意防范投资风
险。