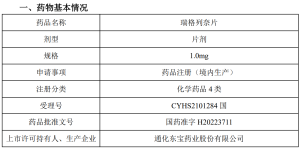
通化东宝:瑞格列奈片获得药品注册证书。
二、研发投入
截至本公告日,通化东宝在该项目中已投入研发费用人民币约 2,536万元。
三、审评结论
根据《中华人民共和国药品管理法》及有关规定,经审查,本品符合药品
注册的有关要求,批准注册,发给药品注册证书。
四、药物研究其他情况说明
瑞格列奈是一种非磺脲类促泌剂,又被称为“餐食血糖调节剂”,能够较
好的对血糖进行控制,尤其是降低餐后血糖,同时其安全性和耐受性较好。在
临床上,该产品常单独使用或者与二甲双胍及基础胰岛素等联用,广泛用于 2
型糖尿病患者的降糖治疗。
瑞格列奈片由诺和诺德公司原研开发,1997 年 12 月经美国 FDA 批准进入临
床,用于饮食控制及运动锻炼不能有效控制高血糖的 2 型糖尿病(非胰岛素依
赖性)患者。现已在英国、德国、中国、欧盟等多个国家和地区上市,我国于
1999 年获得原 CFDA(现 NMPA)的批准上市,进口制剂商品名为诺和龙®。
公司于 2021 年 5 月向国家药品监督管理局药品审评中心递交了药品注册上
市许可申请,2021 年 6 月获得受理,2022 年 10 月收到瑞格列奈片《药品注册
证书》。本次瑞格列奈片以化学药品新注册分类 4 类获批上市,标志着此产品视
同通过仿制药一致性评价。此外,该产品已通过仿制药一致性评价的其他企业
为江苏豪森、北京福元、北京北陆。
五、药品的市场状况
目前,瑞格列奈片的市场仍由原研产品主导,根据米内网 2021 年的最新数
据显示,中国城市公立医院、县级公立医院、城市社区中心及乡镇卫生院(简
称中国公立医疗机构)终端销售额超过 16 亿元,其中原研厂家市场份额占比
51.55%,中国城市实体药店终端销售额为4.1亿元,其中原研厂家市场份额占比
80.82%。但是随着 2021 年 2 月,该产品被纳入了第四批国家集中带量采购目录,
预示着国产仿制产品的市场份额将呈现上升趋势并逐步替代进口原研厂家。